Selamat Datang kembali di blog freemathlearn. Blog yang membahas seputar matematika dan ilmu sains lainnya. Baiklah untuk kali ini akan kita bahas mengenai
Soal Pilihan Ganda Mengenai Sistem Periodik Unsur. Silakan disimak ya guys!
>
Nah itulah tadi telah diuraikan mengenai Soal Pilihan Ganda Mengenai Sistem Periodik Unsur. Bagaimana, silakan berkomentar atau kritik, saran ataupun tambahan dari kamu. Kita tahu kita bukan yang sempurna, siapa tahu kamu lebih dan bisa berbagi. Ditunggu komentarnya guys.
>
Loading...
Soal 1
Pengelompokkan unsur - unsur dilakukan pertama kali oleh . . . . .
A. Dobereiner
B. D.I. Mendeleev
C. Henry G.J. Moseley
D. Jonh Newlands
E. Lothar Meyer
Soal 2
Massa atom unsur klorin, bromin dan iodin berturut turtu adalah 35, 80 dan 127. Ketiganya disusun berdasarkan kenaikan massa atom, maka ketiganya memiliki persamaan . . . . .
A. Massa jenis
B. Titik didih
C. Titik leleh
D. Sifat fisis dan kimia
E. Sifat Intrinsik
Soal 3
Hasil peneglompokan unsur berdasarkan pada sifat fisis dan sifat kimia yang dihubungkan dengan massa atom unsur dikemukakan oleh . . . . .
A. Dobereiner
B. D.I. Mendeleev
C. Henry G.J. Moseley
D. Jonh Newlands
E. Lothar Meyer
Soal 4
Kelemahan penyusunan atom berdasarkan teori oktaf Newland adalah . . . . .
A. Terdapat beberapa atom yang memiliki massa lebih tinggi berada pada urutan yang lebih rendah
B. Urutan kenaikan massa atom tidak kontinu
C. Beberapa unsur yang menurut hitungan terdapat pada satu kelompok, tetapi sifatnya tidak sama
D. Penyusunan berdasarkan kenaikan massa atom banyak kelemahannnya
E. Sistem oktaf hanya berlaku untuk unsur unsur dengan nomor massa kecil
Soal 5
Kelebihan pengelompokan unsur Mendeleev adalah . . . .
A. semua unsur tidak ada yang tidak memiliki tempat
B. Semua unsur dalam satu golongan mempunyai sifat yang sama
C. Diprediksinya suatu unsur yang saat itu belum ditemukan
D. Dalam satu periode tidak ada unsur yang memiliki nomor massa lebih kecil berada di belakang unsur yang memiliki nomor massa lebih besar.
E. Penempatan unsur unsur jadi lebih pendek / sederhana
Soal 6
Dua tokoh yang mencoba mengelompokkan unsur unsur dengan pijakan berbeda, yaitu keniakan massa atom dan kenaikan massa jenis atom, tetapi mendapatkan peneglompokkan yang hampir sama adalah . . . . .
A. John Newlands dan Mendeleev
B. Lothar Meyer dan Mendeleev
C. Moseley dan Mendeleev
D. John Newland dan Dobereiner
E. John Newlands dan Lothar Meyer
Soal 7
Jika kita melihat sistem periodik Mendeleev terdapat beberapa ramalan berdasarkan . . . . .
A. Sifat fisis unsur dalam satu golongan
B. Pembagian massa atom sebelum dan sesudah unsur tersebut dalam satu golongan.
C. Kereaktifan terhadap zat zat tertentu
D. Jumlah protonnnya
E. Massa jenis zat dalam satu golongan
Soal 8
Kelemahan sistem periodik Mendeleev adalah . . . . .
A. Tidak dapat dibedakan golongan dalam SPU Mendeleev
B. Terdapat banyak ruang kosong karena unsurnya belum ditemukan
C. Tidak dicantumkannya fase pada suhu kamar
D. Tidak dibedakan antara padatan dengan cairan
E. Tidak terdapat semua informasi yang diperlukan
Soal 9
Hukum periodik yang menyatakan sifat unsur merupakan fungsi periodik dari nomor atom adalah . . . . .
A. triade dobereiner
B. sistem oktaf Newlands
C. sistem periodik Mendeleev
D. sistem periodik modern (Moseley dan Lothar Meyer)
E. Sistem periodik bentuk pendek
Soal 10
Perbedaan sistem periodik modern dengan peneglompokan unsur sebelumnya adalah . . . . .
A. Perbedaan menempatkan unsur dalam satu periode
B. Perbedaan menemptakan unsur dalam satu golongan
C. SPU modern disusun berdasarkan kenaikan nomor atom
D. SPU modern disusun menjadi 18 golongan
E. SPU modrn disebut SPU panjang
Tipe Soal Analisa
Soal 1
Penyusunan unsur pertama kali dilakukan dengan mengurutkan unsur unsur berdasarkan kanaikan massa atomnya menjadi tiga - tiga. Menurut cara pengelompokan tersebut, jika unsur A massa atomnya 16, unsur C massa atomnya 23, maka unsur B massa atomnya adalah . . . . .
A. 17
B. 19
C. 21
D. 27
E. 28
Soal 2
Diketahui 10 unsur diurutkan menurut kenaikan nomor massanya sebagai berikut.
Yang benar menurut teori oktaf adalah . . . . .
A. H memiliki sifat yang sama dengan Na
B. Li memiliki sifat yang sama dengan Na
C. Be memiliki sifat yang sama dengan F
D. B memiliki sifat yang sama dengan Mg
E. C memiliki sifat yang sama dengan N
INDIKATOR 4
Soal Menentukan Letak Unsur Dalam Sistem Periodik Menggunakan Konfigurasi Atom Bohr
Soal 1
Dibawah ini yang bukan merupakan golongan pada SPU modern adalah . . . .
A. Golongan IA: alkali
B. Golongan IIA : alkali tanah
C. Golongan VA : Nitrogen
D. Golongan VIA : Halogen
E. Golongan VIIIA : gas mulia
Soal 2
Perioda dalam sistem periodik unsur, menyatakan banyaknya . . . .
A. elektron pada kulit terluar
B. neutron dalam inti
C. kulit atom
D. elektron dalam atom
E. proton dalam inti
Soal 3
Suatu unsur memiliki konfigurasi elektron 2 8 18 5. Unsur tersebut terletak pada golongan . . . . .
A. IA
B. VA
C. VIA
D. VIIA
E. VIIIA
Soal 4
Unsur dengan konfigurasi elektron 2 8 5 terletak pada periode . . . . .
A. 2
B. 3
C. 5
D. 6
E. 8
Soal 5
Ion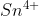 mempunyai konfigurasi elektron 2 8 18 18. Unsur tersebut terletak pada periode . . . .
mempunyai konfigurasi elektron 2 8 18 18. Unsur tersebut terletak pada periode . . . .
A. 3
B. 4
C. 5
D. 6
E. 7
Soal 6
Konfigurasi elektron unsur X adalah 2 8 18 18 5. Unsur tersebut terletak pada . . . .
A. golongan IIA, periode 5
B. golongan VA, periode 5
C. golongan Va, periode 3
D. golongan IIIA, periode 4
E. golongan VIA, periode 5
Soal 7
Anion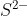 memilki konfigurasi elektron 2 8 8. Atom unsur tersebut terletak pada . . . .
memilki konfigurasi elektron 2 8 8. Atom unsur tersebut terletak pada . . . .
A. golongan IIA, periode 4
B. golongan IIA, periode 8
C. golongan VIA, periode 4
D. golongan VAA, periode 3
E. golongan VIIIA, periode 3
Soal 8
Suatu atom memiliki nomor atom 38 dan memiliki jumlah neutron 50. Unsur tersebut terletak pada . . . .
A. golongan IA, periode 6
B. golongan IIA, periode 5
C. golongan VIA, periode 1
D. golongan VIIA, periode 3
E. golongan VIIA, periode 5
Soal 9
Suatu atom terletak pada golongan III A periode 4, maka konfigurasi elektron unsur tersebut adalah . . . .
A. 2 8 4
B. 2 18 4
C. 2 8 8 3
D. 2 8 18 3
E. 2 18 8 3
Soal 10
Suatu unsur terletak pada golongan VIIA periode 5. Jika nomor massa atom tersebut 127, maka jumlah neutron unsur tersebut adalah . . . . .
A. 43
B. 53
C. 64
D. 67
E. 74
Soal 11
Salah satu ciri ciri unsur golongan halogen adalah . . . . .
A. elektron valensinya 5
B. elektron valensinya 7
C. elektron valensinya 8
D. memiliki jumlah proton = elektron
E. memiliki jumlah elektron > neutronnya
Soal 12
Di bawah ini yang bukan merupakan unsur - unsur golongan alkali adalah . . . . .
A. hidrogen
B. litium
C. natrium
D. kalium
E. rubidium
Soal 13
Unsur transisi dalam SPU dimulai dari periode . . . .
A. 2
B. 3
C. 4
D. 5
E. 6
Soal 14
Banyaknya unsur transisi pada periode keempat adalah . . . . .
A. 8
B. 10
C. 18
D. 32
E. 64
Soal 15
Perbedaan sifat unsur transisi dibandingkan dengan unsur golongan utama adalah . . . . .
A. Fe, Co, Ni, Cu
B. Rb, Sr, Y, Zr
C. Nb, Mo, Tc, Rn
D. Pt, Au, Hg, Tl
E. Th, Pa, U, Np
Menentukan Letak Unsur Dalam Sistem Periodik Menggunakan Konfigurasi Elektron Mekanika Kuantum (subkulit)
Soal 1
Suatu atom X memiliki massa atom realtif 35 dan 18 neutron. Atom X dalam sistem periodik terletak pada . . . . .
A. golongan IA perioda 3
B. golongan IVA perioda 4
C. golongan VIIIA perioda 3
D. golongan VIIA perioda 3
E. golongan IIA perioda 4
(UN Kimia 2006)
Soal 2
Perhatikan tabel sistem periodik unsur berikut!
Konfigurasi elektron unsur R yang paling tepat adalah . . . . .
A. 1s2 2s2 2p6 3s2
B. 1s2 2s2 2p6 3s2 3p6 4s1
C. 1s2 2s2 2p6 3s1
D. 1s2 2s2 2p6 3s2 3p6 3d1
E. 1s2 2s2 2p6 3s2 3p6
(UN Kimia 2014)
Soal 3
Dibawah ini adalah tabel lambang unsur dengan nomor atomnya.
Pasangan unsur yang termasuk ke dalam blok d adalah . . . .
A. P dan S
B. Q dan R
C. Q dan S
D. R dan T
E. P dan R
(Soal EBTASNAS 1998)
Soal 4
Elektron terakhir dari suatu atom menempati bilangan kuantum n = 3, l = 1, m = 0, s = 1/2. Dalam tabel periodik unsur tersebut terletak pada . . . .
A. Golongan VA, periode 2
B. Golongan IVA, periode 3
C. Golongan VIIA, periode 2
D. Golongan VIIA, periode 3
E. Golongan VIIIA, periode 2
(UM UNDIP 2009)
Soal 5
Dalam sistem berskala unsur, unsur X terletak pada periode ketiga dan golongan 15 atau VA. Dalam keadaan ion, unsur ini isoelektronik dengan unsur gas mulia periode ketiga. Muatan ion X adalah . . . .
A. - 1
B. - 2
C. - 3
D. + 2
E. + 3
(SNMPTN 2010)
Soal 6
Konfigurasi elektron yang benar untuk unsur golongan periode ketiga adalah . . . .
A. 1s2 2s2 2p5
B. 1s2 2s2 2p6 3s2
C. 1s2 2s2 2p6 3s1
D. 1s2 2s2 2p6 3p2 3p1
E. 1s2 2s2 2p6 3p2 3p6
Soal 7
Konfigurasi elektron dari unsur X dalam orbital adalah sebagai berikut.
Didalam tabel periodik, unsur X terletak pada . . . . .
A. Golongan IIA, periode 6
B. Golongan IIIA, periode 5
C. Golongan IVA, perioda 4
D. Golongan VA, perioda 3
E. Golongan VA, peroda 2
Soal 8
Unsur golongan IIB terletak pada blok . . . . .
A. s
B. p
C. d
D. f
E. g
Soal 9
Masing masing unsur A, B, C, D dan E memiliki konfigurasi elektron :
Pasangan yang merupakan unsur segolongan adalah . . . .
A. A dan B
B. A dan C
C. A dan D
D. A dan E
E. D dan E
Soal 10
Elektron terakhir atom X memiliki bilangan kuantum, n = 3, l = 0, m = 0, s = - 1/2. atom X terletak pada golongan . . . . dan perioda . . . .
A. IIA/3
B. IIIA/3
C. IIB/3
D. IIIB/3
E. IVB/3
Soal 11
Unsur X dengan massa atom 56 dan jumlah neutron 30, dalam tabel periodik unsur terletak pada . . . . .
A. Golongan VIB perioda 4
B. Golongan VIIB, perioda 4
C. Golongan VIIA, perioda 4
D. Golongan IVB perioda 6
E. Golongan VB, perioda 4
Soal 12
Diantara unsur berikut ini yang berada pada blok d adalah . . . . .
A. 19A
B. 31B
C. 36C
D. 38D
E. 45E
Soal 13
Suatu unsur memiliki konfigurasi elektron [Kr] 5s2 4d10 5p2. Unsur tersebut terletak pada golongan . . . .
A. IIA
B. IIB
C. IVA
D. IVB
E. VIIB
INDIKATOR 5
Soal 1
Pernyataan berikut yang menggambarkan kecendrungan sifat sifat unsur dari kiri ke kakan pada tabel periodik yang benar adalah . . . .
A. jumlah neutron dalam atom berkurang
B. jumlah proton dalam atom berkurang
C. jumlah elektron pada kulit terluar berkurang
D. Kemampuan unsur menghantarkan arus listrik meningkat
E. Unsur unsur bergeser dari logam menjadi nonlogam
Soal 2
Diantara pernyatan berikut ini yang bukan merupakan sifat periodik unsur adalah . . . . .
A. dari atas ke bawah dalam satu golongan jari jari atomnya semakin besar
B. dari kiri ke kanan dalam satu periode potensial ionisasi semakin besar
C. dari atas ke bawah dalam satu golongan energi ionisasi semakin besar
D. dari kiri ke kanan dalam satu periode afinitas elektronnya semakin besar
E. dari atas ke bawah dalam satu golongan keelektrongetaifan semakinkecil
Soal 3
Pernyataan yang benar mengani sifat sifat unsur dalam satu periode dari kiri ke kanan adalah . . . .
A. sifat logam bertambah
B. muatan inti bertambah
C. muatan inti berkurang
D. energi ionisasi berkurang
E. jumlah proton berkurang
Soal 4
Jari jari unsur golongan IIA secara acak dalam satuan angstrom adalah sebagai berikut : 1, 05 ; 2,00 ; 1,80 ; 2,15 ; 1,50. Dari data tersebut yang merupakan jari jari atom barium adalah . . . . .
A. 2,15
B. 2,00
C. 1,80
D. 1,50
E. 1,25
Soal 5
Unsur A, B, C dan E berturut turut nomor atomnya adalah 7, 12, 15, 33 dan 38. Diantara keempat unsur tersebut yang memiliki jari jari atom terpanjang adalah . . . .
A. E
B. D
C. C
D. B
E. A
Soal 6
Dibawah ini adalah grafik keperiodikan jari jari atom unsur perioda ketiga.
Peyimpangan terjadi pada unsur . . .. .
A. Na'
B. Mg
C. Al
D. P
E. Ar
Soal 7
Jari jari atom terbesar pada unsur periode ketiga adalah natrium. Hal tersebut disebabkan oleh . . . . .
A. Atom Na memiliki jumlah elektron paling banyak
B. Atom Na memiliki jumlah elektron valensi paling sedikit
C. Atom Na merupakan atom yang sangat reaktif
D. Atom Na memiliki kerapatan paling kecil
E. Atom Na adalah atom logam
Soal 8
Jari jari ion positif selalu lebih kecul daripada jari jari atomnya. Hal ini disebabkan oleh . . . . .
A. gaya tarik anatra elektron terluar semakin kuat
B. gaya tarik anatra elektron terluar dan inti semakin lemah
C. semakin sedikitnya jumlah elektron terluar
D. semakin banyaknya elektron yang dilepas
E. semakin banyaknya elektron yang diserap
Soal 9
Energi ionisasi adalah . . . .
A. Kemampuan elektron untuk mengion
B. Kemampuan elektron untuk mebentuk ion positif
C. energi minimum yang diperlukan atom untuk mengion dalam wujud gas
D. energi minimum untuk keperluan membentuk ion positif dalam wujud gas
E. energi potensial suatu atom netral menjadi bermuatan
Soal 10
Umumnya energi ionisasi tingkat pertama lebih kecil dibandingkan energi ionisasi tingkat kedua, ketiga dan seterusnya. Hal itu disebabkan oleh . . . . .
A. elektron yang akan dilepas semakin dekat dengan inti atom
B. elektron yang dilepas semakin jauh dari inti atom
C. elektron yang dilepas semakin banyak
D. elektron yang dilepas semakin tinggi derajat ionisasinya
E. elektron yang ditangkap semakin sedikit.
Soal 11
Diantara unsru berikut yang memiliki energi ionisasi paling kecil adalah . . . . .
A. 9
B. 11
C. 15
D. 19
E. 33
Soal 12
Data energi ionisasi pertama dari berbagai unsur sebagai berikut :
P = 1.000 kJ/mol
Q = 738 kJ/mol
R = 186 kJ/mol
S = 1.012 kJ/mol
T = 1.052 kJ/mol
Unsur unsur tersebut dalam satu periode dari kiri ke kanan adalah . . . . .
A. P, Q, R, S, T
B. P, S, T , R, Q
C. S, P, Q, T, R
D. Q, R, P, S, T
E. P, T, R, Q, S
Soal 13
Afinitas elektron terbesar terletak pada . . . . .
A. Golongan IA
B. Golongan IIA
C. Golongan IIIA
D. Golongan IVA
E. Golongan VA
Soal 14
Suatu unsur yang memiliki keelektronegatifan tinggi, umumnya unsur tersebut mempunyai . . . .
A. afinitas elektron rendah
B. energi ionisasi tinggi
C. jari jari atom besar
D. nomor atom kecil
E. kecendrungan membentuk ion positif
Soal 15
Pernyataan di bawah ini yang benar mengenai tabel periodik adalah . . . .
A. semua golongan mengandung unsur logam maupun non logam
B. pada golongan VII, titik leleh unsur unsurnya meningkat seiring dengan meningkatnya nomor atom
C. pada golongan I, reaktifitas berkurang seiring dengan meningkatnya nomor atom
D. Unsur unsur dalam satu periode semakin bersifat logam seiring dengan meningkatnya nomor atom
E. atom atom dari unsur unsur pada golongan yang sama memiliki jumlah elektron yang sama..
Pengelompokkan unsur - unsur dilakukan pertama kali oleh . . . . .
A. Dobereiner
B. D.I. Mendeleev
C. Henry G.J. Moseley
D. Jonh Newlands
E. Lothar Meyer
Soal 2
Massa atom unsur klorin, bromin dan iodin berturut turtu adalah 35, 80 dan 127. Ketiganya disusun berdasarkan kenaikan massa atom, maka ketiganya memiliki persamaan . . . . .
A. Massa jenis
B. Titik didih
C. Titik leleh
D. Sifat fisis dan kimia
E. Sifat Intrinsik
Soal 3
Hasil peneglompokan unsur berdasarkan pada sifat fisis dan sifat kimia yang dihubungkan dengan massa atom unsur dikemukakan oleh . . . . .
A. Dobereiner
B. D.I. Mendeleev
C. Henry G.J. Moseley
D. Jonh Newlands
E. Lothar Meyer
Soal 4
Kelemahan penyusunan atom berdasarkan teori oktaf Newland adalah . . . . .
A. Terdapat beberapa atom yang memiliki massa lebih tinggi berada pada urutan yang lebih rendah
B. Urutan kenaikan massa atom tidak kontinu
C. Beberapa unsur yang menurut hitungan terdapat pada satu kelompok, tetapi sifatnya tidak sama
D. Penyusunan berdasarkan kenaikan massa atom banyak kelemahannnya
E. Sistem oktaf hanya berlaku untuk unsur unsur dengan nomor massa kecil
Soal 5
Kelebihan pengelompokan unsur Mendeleev adalah . . . .
A. semua unsur tidak ada yang tidak memiliki tempat
B. Semua unsur dalam satu golongan mempunyai sifat yang sama
C. Diprediksinya suatu unsur yang saat itu belum ditemukan
D. Dalam satu periode tidak ada unsur yang memiliki nomor massa lebih kecil berada di belakang unsur yang memiliki nomor massa lebih besar.
E. Penempatan unsur unsur jadi lebih pendek / sederhana
Soal 6
Dua tokoh yang mencoba mengelompokkan unsur unsur dengan pijakan berbeda, yaitu keniakan massa atom dan kenaikan massa jenis atom, tetapi mendapatkan peneglompokkan yang hampir sama adalah . . . . .
A. John Newlands dan Mendeleev
B. Lothar Meyer dan Mendeleev
C. Moseley dan Mendeleev
D. John Newland dan Dobereiner
E. John Newlands dan Lothar Meyer
Soal 7
Jika kita melihat sistem periodik Mendeleev terdapat beberapa ramalan berdasarkan . . . . .
A. Sifat fisis unsur dalam satu golongan
B. Pembagian massa atom sebelum dan sesudah unsur tersebut dalam satu golongan.
C. Kereaktifan terhadap zat zat tertentu
D. Jumlah protonnnya
E. Massa jenis zat dalam satu golongan
Soal 8
Kelemahan sistem periodik Mendeleev adalah . . . . .
A. Tidak dapat dibedakan golongan dalam SPU Mendeleev
B. Terdapat banyak ruang kosong karena unsurnya belum ditemukan
C. Tidak dicantumkannya fase pada suhu kamar
D. Tidak dibedakan antara padatan dengan cairan
E. Tidak terdapat semua informasi yang diperlukan
Soal 9
Hukum periodik yang menyatakan sifat unsur merupakan fungsi periodik dari nomor atom adalah . . . . .
A. triade dobereiner
B. sistem oktaf Newlands
C. sistem periodik Mendeleev
D. sistem periodik modern (Moseley dan Lothar Meyer)
E. Sistem periodik bentuk pendek
Soal 10
Perbedaan sistem periodik modern dengan peneglompokan unsur sebelumnya adalah . . . . .
A. Perbedaan menempatkan unsur dalam satu periode
B. Perbedaan menemptakan unsur dalam satu golongan
C. SPU modern disusun berdasarkan kenaikan nomor atom
D. SPU modern disusun menjadi 18 golongan
E. SPU modrn disebut SPU panjang
Tipe Soal Analisa
Soal 1
Penyusunan unsur pertama kali dilakukan dengan mengurutkan unsur unsur berdasarkan kanaikan massa atomnya menjadi tiga - tiga. Menurut cara pengelompokan tersebut, jika unsur A massa atomnya 16, unsur C massa atomnya 23, maka unsur B massa atomnya adalah . . . . .
A. 17
B. 19
C. 21
D. 27
E. 28
Soal 2
Diketahui 10 unsur diurutkan menurut kenaikan nomor massanya sebagai berikut.
Yang benar menurut teori oktaf adalah . . . . .
A. H memiliki sifat yang sama dengan Na
B. Li memiliki sifat yang sama dengan Na
C. Be memiliki sifat yang sama dengan F
D. B memiliki sifat yang sama dengan Mg
E. C memiliki sifat yang sama dengan N
INDIKATOR 4
Soal Menentukan Letak Unsur Dalam Sistem Periodik Menggunakan Konfigurasi Atom Bohr
Soal 1
Dibawah ini yang bukan merupakan golongan pada SPU modern adalah . . . .
A. Golongan IA: alkali
B. Golongan IIA : alkali tanah
C. Golongan VA : Nitrogen
D. Golongan VIA : Halogen
E. Golongan VIIIA : gas mulia
Soal 2
Perioda dalam sistem periodik unsur, menyatakan banyaknya . . . .
A. elektron pada kulit terluar
B. neutron dalam inti
C. kulit atom
D. elektron dalam atom
E. proton dalam inti
Soal 3
Suatu unsur memiliki konfigurasi elektron 2 8 18 5. Unsur tersebut terletak pada golongan . . . . .
A. IA
B. VA
C. VIA
D. VIIA
E. VIIIA
Soal 4
Unsur dengan konfigurasi elektron 2 8 5 terletak pada periode . . . . .
A. 2
B. 3
C. 5
D. 6
E. 8
Soal 5
Ion
A. 3
B. 4
C. 5
D. 6
E. 7
Soal 6
Konfigurasi elektron unsur X adalah 2 8 18 18 5. Unsur tersebut terletak pada . . . .
A. golongan IIA, periode 5
B. golongan VA, periode 5
C. golongan Va, periode 3
D. golongan IIIA, periode 4
E. golongan VIA, periode 5
Soal 7
Anion
A. golongan IIA, periode 4
B. golongan IIA, periode 8
C. golongan VIA, periode 4
D. golongan VAA, periode 3
E. golongan VIIIA, periode 3
Soal 8
Suatu atom memiliki nomor atom 38 dan memiliki jumlah neutron 50. Unsur tersebut terletak pada . . . .
A. golongan IA, periode 6
B. golongan IIA, periode 5
C. golongan VIA, periode 1
D. golongan VIIA, periode 3
E. golongan VIIA, periode 5
Soal 9
Suatu atom terletak pada golongan III A periode 4, maka konfigurasi elektron unsur tersebut adalah . . . .
A. 2 8 4
B. 2 18 4
C. 2 8 8 3
D. 2 8 18 3
E. 2 18 8 3
Soal 10
Suatu unsur terletak pada golongan VIIA periode 5. Jika nomor massa atom tersebut 127, maka jumlah neutron unsur tersebut adalah . . . . .
A. 43
B. 53
C. 64
D. 67
E. 74
Soal 11
Salah satu ciri ciri unsur golongan halogen adalah . . . . .
A. elektron valensinya 5
B. elektron valensinya 7
C. elektron valensinya 8
D. memiliki jumlah proton = elektron
E. memiliki jumlah elektron > neutronnya
Soal 12
Di bawah ini yang bukan merupakan unsur - unsur golongan alkali adalah . . . . .
A. hidrogen
B. litium
C. natrium
D. kalium
E. rubidium
Soal 13
Unsur transisi dalam SPU dimulai dari periode . . . .
A. 2
B. 3
C. 4
D. 5
E. 6
Soal 14
Banyaknya unsur transisi pada periode keempat adalah . . . . .
A. 8
B. 10
C. 18
D. 32
E. 64
Soal 15
Perbedaan sifat unsur transisi dibandingkan dengan unsur golongan utama adalah . . . . .
A. Fe, Co, Ni, Cu
B. Rb, Sr, Y, Zr
C. Nb, Mo, Tc, Rn
D. Pt, Au, Hg, Tl
E. Th, Pa, U, Np
Menentukan Letak Unsur Dalam Sistem Periodik Menggunakan Konfigurasi Elektron Mekanika Kuantum (subkulit)
Soal 1
Suatu atom X memiliki massa atom realtif 35 dan 18 neutron. Atom X dalam sistem periodik terletak pada . . . . .
A. golongan IA perioda 3
B. golongan IVA perioda 4
C. golongan VIIIA perioda 3
D. golongan VIIA perioda 3
E. golongan IIA perioda 4
(UN Kimia 2006)
Soal 2
Perhatikan tabel sistem periodik unsur berikut!
Konfigurasi elektron unsur R yang paling tepat adalah . . . . .
A. 1s2 2s2 2p6 3s2
B. 1s2 2s2 2p6 3s2 3p6 4s1
C. 1s2 2s2 2p6 3s1
D. 1s2 2s2 2p6 3s2 3p6 3d1
E. 1s2 2s2 2p6 3s2 3p6
(UN Kimia 2014)
Soal 3
Dibawah ini adalah tabel lambang unsur dengan nomor atomnya.
Pasangan unsur yang termasuk ke dalam blok d adalah . . . .
A. P dan S
B. Q dan R
C. Q dan S
D. R dan T
E. P dan R
(Soal EBTASNAS 1998)
Soal 4
Elektron terakhir dari suatu atom menempati bilangan kuantum n = 3, l = 1, m = 0, s = 1/2. Dalam tabel periodik unsur tersebut terletak pada . . . .
A. Golongan VA, periode 2
B. Golongan IVA, periode 3
C. Golongan VIIA, periode 2
D. Golongan VIIA, periode 3
E. Golongan VIIIA, periode 2
(UM UNDIP 2009)
Soal 5
Dalam sistem berskala unsur, unsur X terletak pada periode ketiga dan golongan 15 atau VA. Dalam keadaan ion, unsur ini isoelektronik dengan unsur gas mulia periode ketiga. Muatan ion X adalah . . . .
A. - 1
B. - 2
C. - 3
D. + 2
E. + 3
(SNMPTN 2010)
Soal 6
Konfigurasi elektron yang benar untuk unsur golongan periode ketiga adalah . . . .
A. 1s2 2s2 2p5
B. 1s2 2s2 2p6 3s2
C. 1s2 2s2 2p6 3s1
D. 1s2 2s2 2p6 3p2 3p1
E. 1s2 2s2 2p6 3p2 3p6
Soal 7
Konfigurasi elektron dari unsur X dalam orbital adalah sebagai berikut.
Didalam tabel periodik, unsur X terletak pada . . . . .
A. Golongan IIA, periode 6
B. Golongan IIIA, periode 5
C. Golongan IVA, perioda 4
D. Golongan VA, perioda 3
E. Golongan VA, peroda 2
Soal 8
Unsur golongan IIB terletak pada blok . . . . .
A. s
B. p
C. d
D. f
E. g
Soal 9
Masing masing unsur A, B, C, D dan E memiliki konfigurasi elektron :
Pasangan yang merupakan unsur segolongan adalah . . . .
A. A dan B
B. A dan C
C. A dan D
D. A dan E
E. D dan E
Soal 10
Elektron terakhir atom X memiliki bilangan kuantum, n = 3, l = 0, m = 0, s = - 1/2. atom X terletak pada golongan . . . . dan perioda . . . .
A. IIA/3
B. IIIA/3
C. IIB/3
D. IIIB/3
E. IVB/3
Soal 11
Unsur X dengan massa atom 56 dan jumlah neutron 30, dalam tabel periodik unsur terletak pada . . . . .
A. Golongan VIB perioda 4
B. Golongan VIIB, perioda 4
C. Golongan VIIA, perioda 4
D. Golongan IVB perioda 6
E. Golongan VB, perioda 4
Soal 12
Diantara unsur berikut ini yang berada pada blok d adalah . . . . .
A. 19A
B. 31B
C. 36C
D. 38D
E. 45E
Soal 13
Suatu unsur memiliki konfigurasi elektron [Kr] 5s2 4d10 5p2. Unsur tersebut terletak pada golongan . . . .
A. IIA
B. IIB
C. IVA
D. IVB
E. VIIB
INDIKATOR 5
Soal 1
Pernyataan berikut yang menggambarkan kecendrungan sifat sifat unsur dari kiri ke kakan pada tabel periodik yang benar adalah . . . .
A. jumlah neutron dalam atom berkurang
B. jumlah proton dalam atom berkurang
C. jumlah elektron pada kulit terluar berkurang
D. Kemampuan unsur menghantarkan arus listrik meningkat
E. Unsur unsur bergeser dari logam menjadi nonlogam
Soal 2
Diantara pernyatan berikut ini yang bukan merupakan sifat periodik unsur adalah . . . . .
A. dari atas ke bawah dalam satu golongan jari jari atomnya semakin besar
B. dari kiri ke kanan dalam satu periode potensial ionisasi semakin besar
C. dari atas ke bawah dalam satu golongan energi ionisasi semakin besar
D. dari kiri ke kanan dalam satu periode afinitas elektronnya semakin besar
E. dari atas ke bawah dalam satu golongan keelektrongetaifan semakinkecil
Soal 3
Pernyataan yang benar mengani sifat sifat unsur dalam satu periode dari kiri ke kanan adalah . . . .
A. sifat logam bertambah
B. muatan inti bertambah
C. muatan inti berkurang
D. energi ionisasi berkurang
E. jumlah proton berkurang
Soal 4
Jari jari unsur golongan IIA secara acak dalam satuan angstrom adalah sebagai berikut : 1, 05 ; 2,00 ; 1,80 ; 2,15 ; 1,50. Dari data tersebut yang merupakan jari jari atom barium adalah . . . . .
A. 2,15
B. 2,00
C. 1,80
D. 1,50
E. 1,25
Soal 5
Unsur A, B, C dan E berturut turut nomor atomnya adalah 7, 12, 15, 33 dan 38. Diantara keempat unsur tersebut yang memiliki jari jari atom terpanjang adalah . . . .
A. E
B. D
C. C
D. B
E. A
Soal 6
Dibawah ini adalah grafik keperiodikan jari jari atom unsur perioda ketiga.
Peyimpangan terjadi pada unsur . . .. .
A. Na'
B. Mg
C. Al
D. P
E. Ar
Soal 7
Jari jari atom terbesar pada unsur periode ketiga adalah natrium. Hal tersebut disebabkan oleh . . . . .
A. Atom Na memiliki jumlah elektron paling banyak
B. Atom Na memiliki jumlah elektron valensi paling sedikit
C. Atom Na merupakan atom yang sangat reaktif
D. Atom Na memiliki kerapatan paling kecil
E. Atom Na adalah atom logam
Soal 8
Jari jari ion positif selalu lebih kecul daripada jari jari atomnya. Hal ini disebabkan oleh . . . . .
A. gaya tarik anatra elektron terluar semakin kuat
B. gaya tarik anatra elektron terluar dan inti semakin lemah
C. semakin sedikitnya jumlah elektron terluar
D. semakin banyaknya elektron yang dilepas
E. semakin banyaknya elektron yang diserap
Soal 9
Energi ionisasi adalah . . . .
A. Kemampuan elektron untuk mengion
B. Kemampuan elektron untuk mebentuk ion positif
C. energi minimum yang diperlukan atom untuk mengion dalam wujud gas
D. energi minimum untuk keperluan membentuk ion positif dalam wujud gas
E. energi potensial suatu atom netral menjadi bermuatan
Soal 10
Umumnya energi ionisasi tingkat pertama lebih kecil dibandingkan energi ionisasi tingkat kedua, ketiga dan seterusnya. Hal itu disebabkan oleh . . . . .
A. elektron yang akan dilepas semakin dekat dengan inti atom
B. elektron yang dilepas semakin jauh dari inti atom
C. elektron yang dilepas semakin banyak
D. elektron yang dilepas semakin tinggi derajat ionisasinya
E. elektron yang ditangkap semakin sedikit.
Soal 11
Diantara unsru berikut yang memiliki energi ionisasi paling kecil adalah . . . . .
A. 9
B. 11
C. 15
D. 19
E. 33
Soal 12
Data energi ionisasi pertama dari berbagai unsur sebagai berikut :
P = 1.000 kJ/mol
Q = 738 kJ/mol
R = 186 kJ/mol
S = 1.012 kJ/mol
T = 1.052 kJ/mol
Unsur unsur tersebut dalam satu periode dari kiri ke kanan adalah . . . . .
A. P, Q, R, S, T
B. P, S, T , R, Q
C. S, P, Q, T, R
D. Q, R, P, S, T
E. P, T, R, Q, S
Soal 13
Afinitas elektron terbesar terletak pada . . . . .
A. Golongan IA
B. Golongan IIA
C. Golongan IIIA
D. Golongan IVA
E. Golongan VA
Soal 14
Suatu unsur yang memiliki keelektronegatifan tinggi, umumnya unsur tersebut mempunyai . . . .
A. afinitas elektron rendah
B. energi ionisasi tinggi
C. jari jari atom besar
D. nomor atom kecil
E. kecendrungan membentuk ion positif
Soal 15
Pernyataan di bawah ini yang benar mengenai tabel periodik adalah . . . .
A. semua golongan mengandung unsur logam maupun non logam
B. pada golongan VII, titik leleh unsur unsurnya meningkat seiring dengan meningkatnya nomor atom
C. pada golongan I, reaktifitas berkurang seiring dengan meningkatnya nomor atom
D. Unsur unsur dalam satu periode semakin bersifat logam seiring dengan meningkatnya nomor atom
E. atom atom dari unsur unsur pada golongan yang sama memiliki jumlah elektron yang sama..
Nah itulah tadi telah diuraikan mengenai Soal Pilihan Ganda Mengenai Sistem Periodik Unsur. Bagaimana, silakan berkomentar atau kritik, saran ataupun tambahan dari kamu. Kita tahu kita bukan yang sempurna, siapa tahu kamu lebih dan bisa berbagi. Ditunggu komentarnya guys.
Loading...





