Selamat Datang kembali di blog freemathlearn. Blog yang membahas seputar matematika dan ilmu sains lainnya. Baiklah untuk kali ini akan kita bahas mengenai
Semen dan Calsium Klorida (CaCl2). Silakan disimak ya guys!
>
Nah itulah tadi telah diuraikan mengenai Semen dan Calsium Klorida (CaCl2). Bagaimana, silakan berkomentar atau kritik, saran ataupun tambahan dari kamu. Kita tahu kita bukan yang sempurna, siapa tahu kamu lebih dan bisa berbagi. Ditunggu komentarnya guys.
>
Loading...
Semen (Cement)
Sekitar 1500 tahun sebelum masehi, itulah saat pertama kali orang menyadari bahwa pasta/campuran dari campuran kalsium hidroksida dan pasir bisa dijadikan bahan untuk merekatkan batubara dendan batu bara lainnya atau batu dengan batu lainnya untuk membangun sebuah bangunan.
Material ini secara lambat akan menyerap karbondioksida yang ada diudara, dengan demikian mengubah pasta kalsium hidroksida dan pasir ini menjadi kalsium karbonat kembali yang memiliki sifat keras dan kuat.
Reaksi yang terjadi adalah sebagai berikut :
Ca(OH)2(s) + CO2(g) 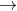 CaCO3(s) + H2O(g)
CaCO3(s) + H2O(g)
Antara 100 tahun sampai 400 tahun sebelum masehi bangsa Roma sudah menggunakan kapur untuk membuat bangunan besar dan saluran air, dan masih banyak diantara bangunan bangsa roma tersebut yang masih berdiri hingga sekarang. Bangsa roma juga kemudian membuat penemuan penting lainnya, yaitu campuran antara debu vulkanik dengan pasir kapur akan meberikan produk yang jauh lebih kuat dibandingkan campuran sebelumnya. Material baru ini kemudian dikenal dengan nama semen pada jaman sekarang.
Produksi semen adalah salah satu produksi terbesar dalam industri kimia saat ini. Secara keseluruhan, didunia telah diproduksi sekitar 700 juta ton semen pertahun dan 10% nya dari jumlah tersebut diproduksi di Amerika. Semen itu dibuat dengan campuran gilingan batu kapur dab shale (campuran dari aluminosilikat) dan dipanaskan sampai suhu 1500 derajat Celsius. Reaksi kimia yang terjadi akan melepasakan karbon dioksida dari campuran dan melelehkan bahan campuran tadi membentuk bubuk padat yang dinamakan arang besi.
Arang besi padat ini kemudian digiling menjadi bubuk dan sedikit kalsium sulfat ditambahkan kedalamnya. Campuran ini dikenal dengan nama "Semen Portland". Secara kimia semen itu mengandung 26 % dikalsium silikat (Ca2SiO4) , 51 % trikalsium silikat 9Ca3SiO4) dan 11% trikalsium aluminat(Ca3Al2O6). Ketika air ditambahkan pada semen, terbentuklah seyawa hidrat yang kompleks. Reaksi kimia yang terjadi seperti berikut :
2CaSiO4(s) + 4H2O(s) 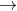 Ca3Si2O7.3H2O + 3H2O(g) + Ca(OH)2(s)
Ca3Si2O7.3H2O + 3H2O(g) + Ca(OH)2(s)
Hidrat silikat yang diebentuk disebut gel "Tobermonter" dan akan membentuk krital yang kuat. Kristal kuat yang dimaksutkan adalah ikatan antara silikon dan oksigen yang kuat yang ada pada pasir dan batu kecil yang dicampurkan pada semen. Karena produk lain dari reaksi diatas adalah kalsium hidroksida campuran ini tentu akan bersifat sangat korosif jika dalam bentuk cair. Untungnya sifat korosifnya akan berkurang ketika campuran ini mengeras.
Kalsium Klorida (CaCl2)
Kalsium klorida anhidrat adalah padatan putih yang sangat mudah menyerap uap air. Karena sifat inilah kadang kadang kalsium klrorida digunakan sebagai zat pengering dilaoratorium. Reaksinya ketika menyerap air akan mebentuk heksahidrat, CaCl2.6H2O dan pemebntukannnya sangat eksotermis sehingga sifat ini akan dimanfaatkan secara komersial. Salah satunya adalah sebagai bahan pengisi "Hot Pack" untuk menghangatkan tangan di negara negara yang bermusim dingin.
Hot Pack itu mengandung dua buah kanton dalam, yang satu berisi air dan yang lain berisi kslium klorida anhidrat, Ketika seseorang meremas Hot Packnya maka kanton yang menampung kalsium kalorida anhidrta akan pecah dan bereaksi dengan air. Akibatnya terbentuklah senyawa hidrat kalsium klorida dan reaksi ini sangat eksotermis sehingga melepaskan panas. Panas inilah yang digunakan orang untuk menghangatkan tangan.
Kalsium klorida anhidrat juga dugunakan sebagai pengganti natrium klorida untuk melelehkan es. Kalisum klorida dalam melelehkan es akan bekerja dalam dua cara. Pertama reaksi denga air akan sangat eksotermis dan kedua kalsium klorida akan mebentuk campuran beku yang secara pasti akan menguragi titik leleh.
Kalsium klorida adalah senyawa yang sangat alrut dalam air. Campuran 30% kalsium kloridan dan 70 % air akan membuat suhu air menurun hingga - 55 derajat Celsius dan ini - 18 derajat Celsius lebih reandah dibandingkan campuran natrium klorida dengan air. Keuntungan alain menggunakan garam kalsium adalah karena karena ion kalsium memiliki dampak yang sedikit terhadap kesehatan dibandingkan ion natrium.
Larutan kalsium klorida pekat adalah larutan yang sangat lengket dan sifat ini dimanfaatkan orang untuk keperluan lain. Jika larutan ini disemprotkan kepermukaan jalan maka akan mengurangi dampak berbahaya jalan dibandingkan menggunakan minyak karena tidak baik terhadap lingkungan. Larutan kalsium klorida jungan sangat berat , dan untuk beberapa alasan kadang kadang larutan ini digunakan untuk mengisi ban alat berat untuk memebikan massa yang lebih berat sehingga fungsinya jauh lebih baik.
.
Nah itulah tadi telah diuraikan mengenai Semen dan Calsium Klorida (CaCl2). Bagaimana, silakan berkomentar atau kritik, saran ataupun tambahan dari kamu. Kita tahu kita bukan yang sempurna, siapa tahu kamu lebih dan bisa berbagi. Ditunggu komentarnya guys.
Loading...



